9 de marzo de 2021
Argentina se suma a los ensayos clínicos de la vacuna alemana CureVac
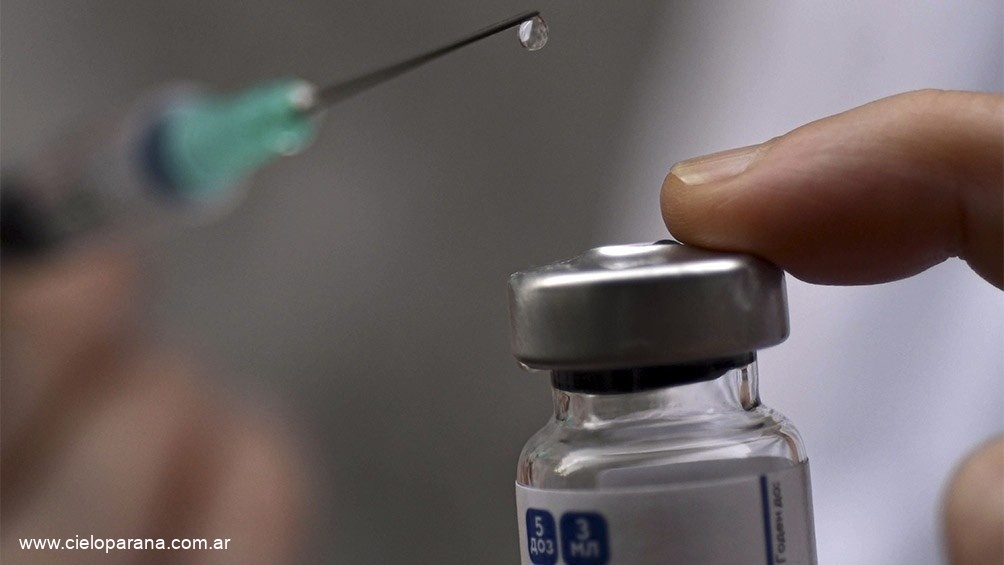
Se trata de los ensayos clínicos en Fase 3 de esta vacuna contra el coronavirus, que comenzaron este lunes en el país. Ya llevan 13 mil vacunados en el mundo.
 De los 13 mil voluntarios vacunados con CureVac, ninguno presentó complicaciones graves.
De los 13 mil voluntarios vacunados con CureVac, ninguno presentó complicaciones graves.El doctor Juan Marini, director ejecutivo del Hospital Evita Pueblo de Berazategui y coordinador de los ensayos clínicos en Fase 3 de la vacuna alemana contra el coronavirus CureVac-004, que comenzaron este lunes en el país, aseguró a Télam que calculan que "en un mes estaríamos terminando las pruebas en la Argentina y en el mundo, y estaríamos en condiciones de verificar su efectividad".
"En este momento ya llevamos 13 mil vacunados en todo el mundo, en mayor cantidad en Europa, en países como Holanda, Bélgica y Alemania, y en número más reducido en América, en México y Perú donde se comenzó con los ensayos", explicó Marini.
"De estos 13 mil, ninguno presentó complicaciones graves. De ahí que se plantea -como ya se presentó en la Fase 2B- como una vacuna segura y veremos su eficacia cuando termine la Fase 3, si es del es del 92, 94 o 96%", indicó.
El director del Hospital Evita Pueblo explicó a Télam que "siendo esta una vacuna que se desarrolló siguiendo el principio de ARN Mensajero -la misma que emplean otras como Pfizer o Moderna- tiene con ellas algunas diferencias, aunque no sustanciales".
"Una diferencia es que necesita una menor dosis de componente. Mientras que la vacuna CureVac necesita 12 microcramos, la de Pfizer necesita 30 y la de Moderna 100. Esto significa que se pueden producir más cantidad de vacunas en menor tiempo", aclaró Marini.
Con respecto a la temperatura, el investigador señaló que todas estas vacunas necesitan una temperatura de -70 grados, pero en el caso de la CureVac, después tiene la posibilidad de estar unas 16 horas en una temperatura de heladera común, "un tiempo muy apropiado y práctico para su operatividad", aseguró.
"Lo que nos preocupa a todos es la aparición de las nuevas cepas, sean las de Brasil (una en Manaos y otra distinta en San Pablo), las de África de las que no se sabe mucho y la del Reino Unido, aunque de esta última se conoce un poco más y sabemos que cualquier vacuna las está cubriendo. Sin contar que no sabemos si habrá más mutaciones más adelante", agregó.
De ahí que Marini celebre como "muy bienvenidas" las nuevas investigaciones y ensayos clínicos de nuevas vacunas.
Voluntarios para el ensayo de CureVac
Este lunes, el Ministerio de Salud de la Provincia de Buenos Aires abrió la inscripción para participar de los ensayos clínicos (Fase 3) de esta vacuna, que pretende evaluar la eficacia en dos dosis para la prevención de casos graves de Covid-19 confirmados por virología y en sujetos sin tratamiento previo, bajo la coordinación general del hospital Evita Pueblo de la localidad bonaerense de Berazategui.
"Se trata de un estudio aleatorizado doble ciego, es decir que los y las voluntarias reciben el placebo o la vacuna al azar, en el que tanto participantes como investigadores no saben qué sustancia fue aplicada en cada caso", explicó Marini.
Se espera que, con 9 mil voluntarios, Argentina se sume a Alemania, Holanda, Bélgica, México, Colombia, Panamá y Perú, donde ya se encuentran realizando los ensayos clínicos de Fase 3 de esta vacuna.
 El Ministerio de Salud de la Provincia de Buenos Aires abrió la inscripción para participar de los ensayos clínicos (Fase 3)
El Ministerio de Salud de la Provincia de Buenos Aires abrió la inscripción para participar de los ensayos clínicos (Fase 3)Las personas que deseen ser voluntarias de este estudio tienen que ser mayores de edad y no estar bajo tratamiento oncológico o inmunodeprimidos, y en el caso de las mujeres no pueden estar embarazadas ni tener planes de estarlo durante el próximo año, ni estar atravesando el periodo de lactancia.
Por otra parte, Marini dijo que es "importante decir que si durante el ensayo clínico quedase demostrada la eficacia de la vacuna, se suspenderá el testeo ciego y todos los voluntarios que recibieron placebo tendrán derecho a ser vacunados por CureVac. Es decir que los 9 mil van a recibir la vacuna dentro de los tres meses".
Una vez finalizado el periodo de inscripción de voluntarios, que comenzó este lunes y se extenderá por 30 días, las pruebas se llevarán a cabo en algunos hospitales bonaerenses, públicos y privados, y también se sumarán dos centros, uno en Rosario y otro la Ciudad de Buenos Aires.
Para la inscripción cada hospital o centro de salud dispondrá un call center y difundirá información en su página web.
Por su parte, desde Mar del Plata, el director del Instituto de Investigaciones Clínicas (IIC), Ignacio Mackinnon, dijo a una radio local que su institución será una de las sedes “en las próximas semanas" del ensayo clínico de Fase 3 de la vacuna CureVac-004.
El desarrollo de CureVac
La vacuna del laboratorio CureVac fue desarrollada con el apoyo del gobierno alemán y la Comunidad Europea y pasó exitosamente los ensayos de las fases 1 y 2 y, una vez aprobada esta última fase y puesta en el mercado, Laboratorios Bayer será quien asuma la fármaco-vigilancia de la tecnología y participará del proceso de producción y distribución a escala.
Desde la corporación farmacéutica aseguran que están en condiciones de fabricar 160 millones de dosis durante 2021.
Los laboratorios buscan la realización de esta clase de estudios en naciones con una circulación viral alta y con buenas capacidades tecnológicas instaladas, mientras que los gobiernos planean negociar, luego, un acceso diferencial a las vacunas.
Otras empresas biotecnológicas han desarrollado sus ensayos clínicos en Argentina como Pfizer, cuyas pruebas -con miles de voluntarios- se desarrollaron en el Hospital Militar de la ciudad de Buenos Aires, donde fueron coordinadas por el médico Fernando Polack.
También la de Sinopharm, que se llevó a cabo por iniciativa de la Fundación Huésped y la supervisión de Pedro Cahn.
COMPARTIR:
Comentarios
Aun no hay comentarios, sé el primero en escribir uno!

:quality(85)/cloudfront-us-east-1.images.arcpublishing.com/infobae/SPDMQLJUQFFSPNKZBA3WTWA5BI.jpg)
:quality(85)/cloudfront-us-east-1.images.arcpublishing.com/infobae/APVCIQ64OZB6VM3N55LGESQCEE.jpg)
:quality(85)/cloudfront-us-east-1.images.arcpublishing.com/infobae/W5ZTCI5RJS33K5HJ7PAHKAR5PQ.jpg)
:quality(85)/cloudfront-us-east-1.images.arcpublishing.com/infobae/TQRGGHIHB5EIVNCD5SQ3SNJVMM.jpg)
:quality(85)/cloudfront-us-east-1.images.arcpublishing.com/infobae/LOVI6E3ZUNDVPI7V4W5NMFUW3Y.jpg)
:quality(85)/cloudfront-us-east-1.images.arcpublishing.com/infobae/XH5BDPH5S7SJIVN6JHM45URVPA.jpg)
:quality(85)/cloudfront-us-east-1.images.arcpublishing.com/infobae/2SLW27OHGNCO3ICOGDEWXR2WIM.jpg)
:quality(85)/cloudfront-us-east-1.images.arcpublishing.com/infobae/KRYHRASW6NAALHVXEJF7VMIIZ4.jpg)